(译文)益生菌脆弱拟杆菌BF839在肿瘤免疫治疗中的临床应用前景
原文链接:https://www.frontiersin.org/journals/microbiology/articles/10.3389/fmicb.2025.1523754/full
彭昆伟1,2,3† 李宇清1,2,3† Qijun Yang 1,2,3 Peijin Yu 1,2,3 曾婷4 林楚慧4
邓宇虹4* 陈静琦1,2,3*
1广州医科大学附属第二医院肿瘤内科(广州510260)
2广州市纳米生物医学诊断与治疗技术研发重点实验室(广州510260)
3广东省教育厅肿瘤微环境纳米免疫调控重点实验室(广州510260)
4广州医科大学附属第二医院临床营养科(广州510260)
【摘要】
研究背景:现有充分证据表明肠道微生物群可调控肿瘤对免疫检查点抑制剂(immune checkpoint inhibitors, ICIs)的治疗应答。益生菌株脆弱拟杆菌BF839(Bacteroides fragilis BF839)在中国临床实践中已广泛应用于肠道菌群失调相关症状的改善。本研究提出BF839可能增强肿瘤对ICIs敏感性的科学假设。
方法:在临床前研究中,小鼠分别接受口服BF839、腹腔注射PD-1抑制剂或两种药物的联合治疗。通过评估肿瘤生长情况和肿瘤免疫微环境来研究BF839的抗肿瘤效果。收集小鼠粪便样本进行16S rRNA测序,新鲜肿瘤组织样本进行16S RNA测序。同时回顾性分析了29例接受BF839辅助治疗的晚期实体瘤患者的临床数据,主要终点为总生存期(OS)。
结果:在接受免疫检查点抑制剂(ICIs)联合化疗的晚期实体瘤患者中,长期BF839辅助治疗组患者的总生存期显著长于短期治疗组(p=0.0101)。临床前研究显示,单独使用BF839或抗PD-1抗体均能显著抑制肿瘤生长。值得注意的是,BF839与抗PD-1抗体具有协同作用,通过增加CD8+T细胞浸润介导了肿瘤消退。机制研究表明,BF839诱导的肿瘤抑制效应是通过cGAS-STING信号通路调控的。小鼠粪便16S rRNA测序结果显示,BF839治疗显著提高了肠道菌群多样性。
结论:本研究证实BF839通过激活cGAS-STING信号通路增强肿瘤对ICIs的敏感性。未来应用益生菌BF839调节肠道菌群可能成为增强ICIs疗效的新策略。
1引言
近年来,靶向程序性细胞死亡蛋白1(PD-1)、程序性死亡配体1(PD-L1)和细胞毒性T淋巴细胞相关蛋白4(CTLA-4)等免疫检查点的单克隆抗体类免疫检查点抑制剂(ICIs)已彻底改变多种癌症的治疗格局(Kennedy and Salama, 2020)。美国食品药品监督管理局(FDA)已批准ICIs用于非小细胞肺癌(NSCLC)、肝细胞癌(HCC)、鼻咽癌、三阴性乳腺癌、高微卫星不稳定性(MSI-H)肿瘤等适应症(Forde et al., 2022; Qin et al., 2023; Chan et al., 2023; Cortes et al., 2022; Ludford et al., 2023)。现有研究证实,肿瘤免疫治疗主要通过激活或重建宿主免疫系统来抑制或杀伤癌细胞,具有毒性低、效率高等优势(Yang, 2015)。但需注意,相当比例患者对ICIs无应答,需通过联合治疗提升免疫治疗获益。目前联合策略主要集中于化疗、抗血管生成治疗及靶向治疗,但这些方案可能增加不良反应风险(Park et al., 2024; Mok et al., 2024; Motzer et al., 2024)。以益生菌为代表的免疫调节剂已成为当前研究热点(Wang et al., 2018)。
肠道菌群与肠黏膜维持共生关系,在健康个体的代谢调控、免疫调节、肠道屏障保护和肿瘤监测中发挥关键作用(Brezina等,2023;Erttmann等,2022;Liu等,2024)。在抗肿瘤效应方面,肠道菌群介导免疫激活的功能已获实验证实(Li等,2022;Mattiola和Diefenbach,2023)。研究表明,肠道菌群通过代谢和免疫调控机制,其组成/多样性显著影响ICIs的疗效和毒性(Routy等,2018;Hu等,2024)。黑色素瘤患者接受免疫治疗时,肠道菌群构成深刻影响临床应答,而粪便菌群移植可逆转治疗耐药(Davar等,2021;Gopalakrishnan等,2018;Szostak等,2024)。这些发现确立了肠道菌群作为潜在生物标志物和治疗靶点的价值。过去十年间,利用益生菌维持健康菌群以改善肿瘤治疗结局的研究迅速兴起(Zheng等,2020;Tomita等,2020),益生菌辅助治疗已成为增强ICIs疗效的研究热点。
脆弱拟杆菌BF839是1983年9月从健康婴儿肠道分离的革兰阴性杆菌,在我国广泛应用于改善便秘、腹泻等菌群失调症状(Geng等,2023)。已有证据表明,脆弱拟杆菌特异性T细胞应答与CTLA-4阻断疗效相关(Vétizou等,2015)。因此,BF839可能成为改善肿瘤患者免疫治疗结局的新策略。本研究旨在阐明BF839与ICIs敏感性的关系:通过16S rRNA测序和RNA测序解析其调控抗肿瘤免疫的机制;利用B16-STING基因敲除黑色素瘤模型,证实BF839通过cGAS-STING通路抑制肿瘤生长;特别发现BF839与抗PD-1抗体具有协同效应,通过增加CD8+T细胞浸润诱导肿瘤消退。临床观察显示,口服BF839可显著提高晚期实体瘤对ICIs的敏感性。这些发现为临床运用BF839改善肿瘤免疫治疗应答提供了理论依据。
2.方法
2.1细胞系
B16F10(C57BL/6小鼠黑色素瘤)细胞和B16-STING-KO细胞由中山大学肿瘤防治中心的夏小军博士慷慨馈赠。B16-STING-KO细胞是通过CRISPR/Cas9技术在B16F10细胞上稳定敲除STING基因构建而成。所有细胞系均在含有10%胎牛血清(FBS)和1%青霉素-链霉素的RPMI 1640培养基(赛默飞世尔科技公司)中,在37℃、5% CO₂条件下培养。
2.2体内实验处理
六周龄雌性C57BL/6小鼠购自北京斯贝福生物技术有限公司,并饲养于无特定病原体(SPF)环境中。每只小鼠皮下接种黑色素瘤细胞(0.5×10⁶个细胞/只)。在接种黑色素瘤细胞前近1周,将小鼠分别用BF839(3.3 mL/kg,5×10⁶ CFU,灌胃,每日一次)、HK-BF839(60°C热灭活2小时,3.3 mL/kg,灌胃,每日一次)、双歧杆菌四联活菌片(42 mg /只,5×10⁶菌落形成单位,灌胃,每日一次)处理。当肿瘤平均体积达到约200 mm³时,小鼠腹腔注射抗PD-1抗体(100 μg /只,每3天一次)。治疗期间每9天采集3只小鼠的粪便样本,并分笼饲养以减少粪食行为导致的交叉污染。具体治疗方案见图表及图注。肿瘤体积计算公式:0.5×肿瘤长径×(肿瘤短径)²。按说明书对小鼠肿瘤组织进行免疫组化染色,检测CD8⁺T细胞(98941S,CST)和Foxp3⁺T细胞(12653S,CST)。
2.3患者资料
本研究回顾性分析了29例在广州医科大学附属第二医院(中国广东广州)接受益生菌BF839辅助治疗(20 mL/次,1×10^8 CFU,口服,每日一次,图腾生物,中国大连)联合免疫检查点抑制剂及化疗的晚期实体瘤患者。治疗持续至出现不可耐受毒性。BF839辅助治疗时长超过4个月定义为长期治疗组,短于4个月为短期治疗组。生存时间通过患者随访记录核实。
2.4 16S rRNA测序与分析
新鲜粪便样本采集后立即液氮冻存。使用特定带条形码引物对粪便样本提取的DNA进行PCR扩增,通过1%琼脂糖凝胶电泳检测PCR产物片段长度及浓度。根据产物浓度计算各样本混合体积,采用凝胶回收试剂盒纯化混合PCR产物,TE缓冲液回收目标DNA片段。最终使用Illumina Nova 6000测序平台进行250PE双端测序。原始测序数据经质控、过滤及拼接获得高质量clean data,用于后续物种群落分析、多样性分析和差异分析。测序及统计分析由广州美格基因科技有限公司完成。
2.5 RNA测序与生物信息学分析
新鲜肿瘤组织样本采集后立即液氮冻存。使用Trizol试剂盒(美国Invitrogen公司)提取总RNA,通过Agilent 2100生物分析仪(美国安捷伦科技)和RNase-free琼脂糖凝胶电泳检测RNA质量。总RNA提取后,采用Oligo(dT)磁珠富集真核生物mRNA,随后用片段化缓冲液将mRNA随机打断,并利用随机引物反转录为cDNA。以DNA聚合酶I、RNase H、dNTP及缓冲液合成第二链cDNA,经QiaQuick PCR纯化试剂盒(荷兰Qiagen公司)纯化后,进行末端修复、加poly(A)尾并与Illumina测序接头连接。连接产物通过琼脂糖凝胶电泳进行片段选择,PCR扩增后交由广州美格基因科技有限公司使用Illumina novaseq 6000平台进行测序。
采用DESeq2软件进行组间差异表达分析,将错误发现率(FDR)<0.05且绝对倍数变化≥2的基因定义为差异表达基因,并进行GO和KEGG富集分析。通过GSEA软件和MSigDB数据库开展基因集富集分析,检测特定通路基因集的组间显著性差异。具体流程为:输入基因表达矩阵,采用Signal2Noise标准化方法排序基因,按默认参数计算富集分数与p值。
2.6统计学分析
采用描述性统计方法分析人口学资料与临床特征。两组间比较使用双尾非配对Student's t检验,多组比较采用单因素或双因素方差分析(肿瘤生长实验)。α多样性组间差异分析分别进行参数检验与非参数检验:仅两组比较时采用Student's t检验或Wilcoxon秩和检验;多组比较采用Kruskal-Wallis秩和检验或单因素方差分析。β多样性差异分析使用Bray-Curtis算法。设定p<0.05为统计学显著性阈值,其中*表示p<0.05,**表示p<0.01,***表示p<0.001,ns表示p>0.05(无统计学差异)。所有数据分析均通过GraphPad Prism 7软件(GraphPad Software公司)完成。
3结果
3.1患者基线特征
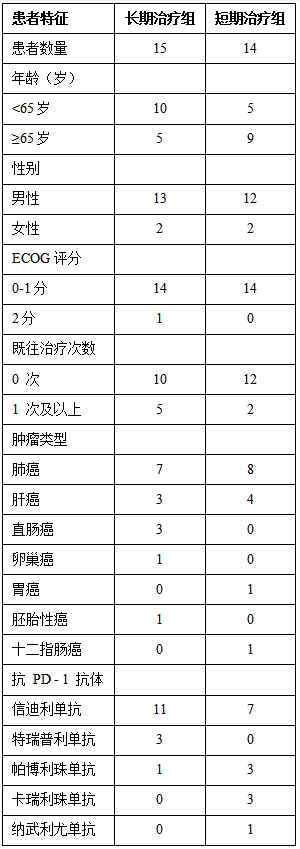
本研究纳入广州医科大学附属第二医院(中国广东广州)29例晚期实体瘤患者。患者基线临床特征详见表1。其中长期治疗组15例(51.72%),短期治疗组14例(48.28%)。年龄<65岁者15例(51.72%),女性患者占比13.78%。病理类型以肺癌为主(15例,51.72%),其次为肝癌(7例,24.14%)。一线治疗患者22例(75.86%),二线及以上治疗7例(24.14%)。美国东部肿瘤协作组(ECOG)体力状态评分0-1分28例(96.55%),2分1例(3.45%)。
表1.患者特征。
3.2长期BF839治疗可延长免疫治疗患者生存期
我们前期研究发现,BF839辅助治疗能显著降低化疗患者不良反应,但不影响化疗疗效(Zeng等,2024)。基于此,我们回顾性分析BF839能否延长接受免疫检查点抑制剂(ICIs)联合化疗患者的生存期。按BF839治疗时长将患者分为两组:长期治疗组(>4个月)和短期治疗组(<4个月)。与短期治疗组相比,长期治疗组患者总生存期(OS)显著延长(p=0.0101,图1A)。短期治疗组中位OS为7.5个月,而长期治疗组未达到中位OS。长期治疗组1年生存率达86.15%,短期治疗组为26.67%;2年生存率分别为51.39%和26.67%。一例肝癌术后肺转移患者接受4周期化疗联合ICIs治疗,每次复查均显示疾病进展(图1B),肿瘤标志物AFP从17,249μg/mL升至62,858μg/mL,被判定为ICIs原发性耐药。在ICIs基础上加用BF839口服治疗1个月后,CT复查显示部分缓解,AFP降至39,564μg/mL(图1C)。
图1
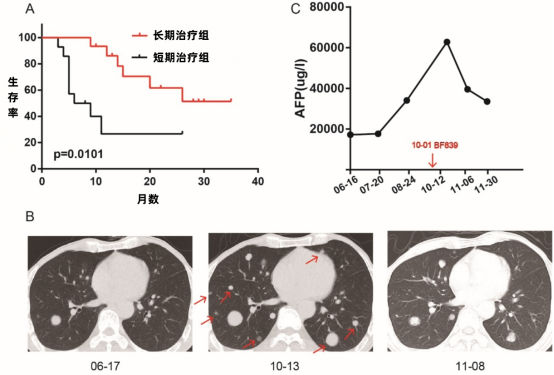
图1.长期口服BF839可改善接受免疫治疗的患者的生存率。(A) BF839短期治疗组与长期治疗组的生存分析。(B) BF839治疗前后典型肺转移病灶的影像学对比。(C) BF839治疗前后甲胎蛋白(AFP)水平变化。
3.3 BF839通过cGAS-STING通路抑制肿瘤生长
本研究采用小鼠黑色素瘤细胞(B16)模型评估BF839、热灭活BF839(HK-BF839)及常用益生菌双歧杆菌(Bifico)的抗肿瘤效应。结果显示,在B16肿瘤细胞接种前1周开始每日口服BF839可显著抑制肿瘤生长(图2A),而HK-BF839无此效应(图2A)。为探究BF839的作用机制,我们对肿瘤组织进行RNA测序分析(对照组vs BF839组),发现BF839组中347个基因表达上调,65个基因表达下调(图2B),差异表达基因热图见补充图S1。对412个差异基因的通路富集分析显示,"免疫系统过程"、"免疫应答"、"防御反应"、"免疫系统调节"及"细菌应答信号通路"显著富集(补充图S2)。基因集富集分析(GSEA)表明,BF839组中"胞质DNA感受(cGAS-STING)通路"显著激活(图2C)。通过构建B16-STING基因敲除(KO)细胞模型进一步验证发现,BF839对B16-STING-KO肿瘤的生长抑制作用消失(图2D),证实BF839通过cGAS-STING通路发挥抗肿瘤效应。
图2
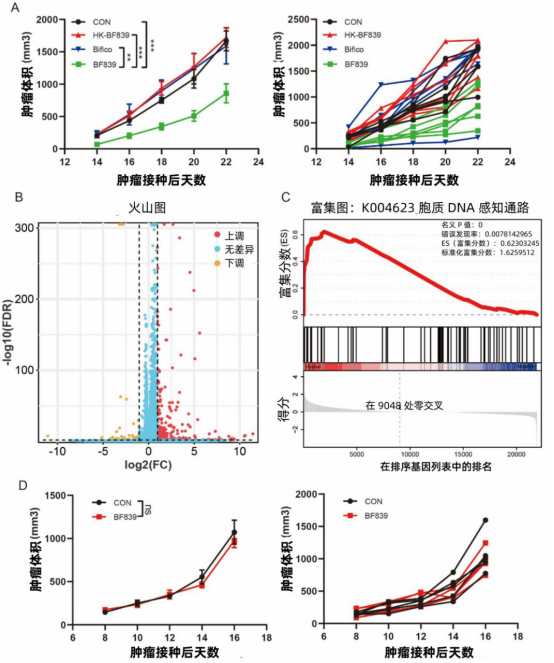
图2. BF839通过cGAS-STING通路抑制肿瘤生长。(A)B16荷瘤小鼠经PBS、BF839、HT-BF839或Bifico处理后的肿瘤体积变化(数据以均值±标准误表示,每组n=6)。(B)RNA-seq分析鉴定PBS组与BF839组间412个差异表达基因。(C)胞质DNA感受(cGAS-STING)通路的GSEA分析结果。(D)B16-STING-KO荷瘤小鼠经PBS或BF839处理后的肿瘤体积变化(数据以均值±标准误表示,每组n=6)。
3.4 BF839促进CD8+T细胞浸润并增强抗PD-1疗法疗效
为探究BF839是否与抗PD-1疗法具有协同效应,我们建立了黑色素瘤小鼠模型。实验将小鼠随机分为四组:对照组、BF839组、抗PD-1组及BF839联合抗PD-1组。在B16肿瘤细胞接种前约1周,BF839组和联合组开始每日口服BF839。当肿瘤平均体积达200mm³时,对相应组别进行抗PD-1抗体腹腔注射。治疗期间每9天采集粪便样本,具体治疗方案详见图3A。
图3
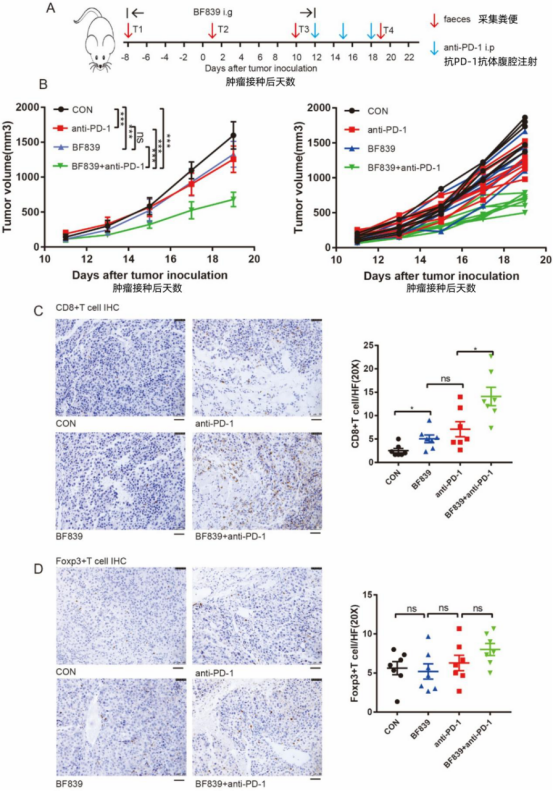
图3. BF839联合抗PD-1治疗促进CD8+T细胞浸润。(A) B16黑色素瘤荷瘤小鼠治疗方案示意图。(B) PBS组、BF839组、抗PD-1组及BF839联合抗PD-1组处理的荷瘤小鼠肿瘤体积变化(数据以均值±标准误表示,每组n=7)。(C)肿瘤组织CD8+T细胞代表性免疫组化染色及定量分析(数据以均值±标准误表示,每组n=7)。标尺:50μm。(D)肿瘤组织Foxp3+T细胞代表性免疫组化染色及定量分析(数据以均值±标准误表示,每组n=7)。标尺:50μm。
研究发现,BF839单菌治疗或抗PD-1抗体单药治疗均能显著抑制肿瘤生长,而BF839可进一步增强抗PD-1抗体的治疗效果(图3B)。为验证BF839对肿瘤微环境的影响,我们对小鼠肿瘤组织进行免疫组化分析。结果显示,BF839治疗能促进肿瘤微环境中CD8+T细胞的浸润,且与抗PD-1抗体联用效果更为显著(图3C),但对Foxp3+T细胞浸润无显著影响(图3D)。这表明BF839与抗PD-1抗体具有协同抗肿瘤效应,其主要通过促进CD8+T细胞浸润发挥作用。
3.5 BF839治疗增加肠道菌群多样性
通过16S rRNA测序分析BF839对小鼠肠道菌群结构的影响。反映菌群多样性的丰富度指数显示,对照组显著低于BF839治疗组(图4A)。虽然抗PD-1抗体治疗组的菌群多样性较对照组有所提高,但差异无统计学意义(图4A)。主坐标分析(PcoA)表明,对照组与BF839治疗组的菌群结构存在显著差异(图4B)。T4.BF组样本分布与T4.BF.PD1组更为接近,提示两组菌群组成相似度较高(图4B)。在科水平上,Muribaculaceae(鼠杆菌科)、Lachnospiraceae(毛螺菌科)、Lactobacillaceae(乳杆菌科)和Ruminococcaceae(瘤胃菌科)为优势菌科(图4C)。属水平分析显示,BF839治疗组的Allobaculum(异杆菌属)丰度较非BF839治疗组降低(图4D)。这些结果证实BF839能有效改善肠道菌群多样性。
图4
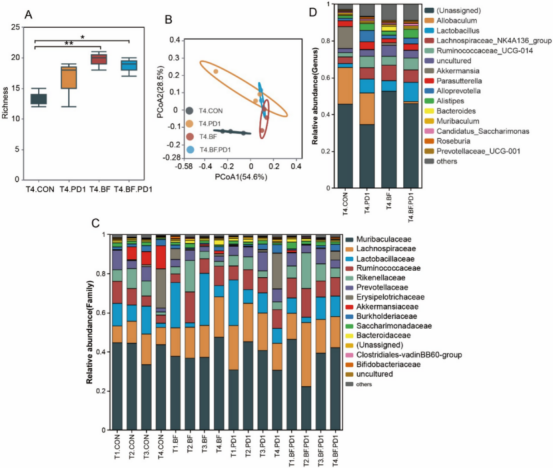
图4展示了BF839治疗对肠道菌群多样性的影响:(A)属水平肠道菌群α多样性分析,显示BF839组较对照组显著提高菌群丰富度;(B)基于Bray-Curtis距离的属水平主坐标分析(PCoA)表明BF839组与对照组菌群结构存在显著分离(ANOSIM p<0.05);(C)科水平菌群组成分析显示Muribaculaceae(鼠杆菌科)、Lachnospiraceae(毛螺菌科)、Lactobacillaceae(乳杆菌科)和Ruminococcaceae(瘤胃菌科)为优势菌群;(D)属水平热图分析显示BF839组Allobaculum(异杆菌属)丰度显著降低(p<0.01)。所有数据均以均值±标准误表示(n=6/组),统计学差异通过Wilcoxon秩和检验确定。
4讨论
大量证据表明益生菌可影响实体瘤的抗肿瘤免疫(Li等,2024;Liu等,2024;Roy和Singh,2024)。本研究的临床前实验表明:BF839联合抗PD-1治疗能显著抑制肿瘤生长,并促进肿瘤微环境中CD8+T细胞浸润。小鼠粪便16S rRNA测序显示,非BF839治疗组的肠道菌群多样性显著低于BF839治疗组。肿瘤组织RNA测序分析表明BF839组中cGAS-STING通路显著激活。此外,本研究揭示了益生菌BF839对晚期实体瘤患者ICI疗效的潜在协同作用。与BF839短期治疗组相比,BF839长期治疗组患者的总生存期更长。长期治疗组的1年生存率为86.15%,短期治疗组为26.67%。长期治疗组的2年生存率为51.39%,短期治疗组为26.67%。这些发现为临床应用BF839改善肿瘤对ICIs的反应提供了强有力的理论依据。
益生菌已被证明有益于人类健康,免疫系统、炎症和消化道疾病会强烈影响肠道菌群(Sehrawat等,2021)。鉴于益生菌治疗可以改善肠道菌群的失衡和多样性,它对肿瘤免疫治疗具有积极作用(Derosa和Zitvogel,2022;Zitvogel等,2022)。目前已发现多种益生菌可以改善免疫治疗效果。有文献记载,益生菌丁酸梭菌(Clostridium butyricum)增强了非小细胞肺癌患者对ICIs的疗效(Tomita等,2020)。CBM588是一种促进双歧杆菌生长的活菌制剂,据报道可以改善接受纳武利尤单抗和伊匹木单抗治疗的转移性肾细胞癌患者的临床结局;接受纳武利尤单抗和伊匹木单抗联合CBM588治疗的患者无进展生存期(12.7个月)显著长于未接受CBM588治疗的患者(2.5个月)(Dizman等,2022)。在另一项研究中,通过口服灌胃给予脆弱拟杆菌增加了肠道菌群多样性和有益共生菌,显著减轻了急慢性移植物抗宿主病(GVHD)的发展(Sofi等,2021)。
肠道菌群可通过多种策略进行调控,其中粪便菌群移植(FMT)作为治疗复发性艰难梭菌感染的安全有效方法,已被应用于肿瘤治疗领域(van Nood等,2013;McQuade等,2019)。一项针对黑色素瘤患者的研究显示,15例对免疫治疗耐药的患者在接受免疫治疗应答者的粪便菌群移植后,其中6例患者重新获得治疗敏感性(Davar等,2021)。另一种策略是细菌基因工程技术,通过改造肠道菌群或其代谢产物可增强对ICIs的抗肿瘤应答(Ma等,2023)。目前,经基因减毒、营养缺陷或诱导型改造的大肠杆菌、双歧杆菌、李斯特菌和沙门氏菌已在临床前模型中显示出抗肿瘤效果(Chang等,2020;Taniguchi等,2016;Liang等,2019;Zhou等,2018;Lee等,2021)。瘤内注射大肠杆菌Nissle 1917可提高细胞内L-精氨酸浓度,诱导CD4+和CD8+T细胞浸润,并与抗PD-L1治疗产生协同抗肿瘤效应(Canale等,2021)。此外,饮食和生活方式的调整也被证实参与肠道菌群调控(Wolter等,2021;Simpson等,2022;Spencer等,2021)。非营养不良性热量限制不仅能降低肿瘤发生风险,还可重塑肠道菌群(Mao等,2023),其机制与乙酸产量增加和干扰素-γ+CD8+T细胞积聚相关。最新研究发现,维生素D水平可通过促进脆弱拟杆菌(Bacteroides fragilis)生长来增强抗肿瘤免疫(Giampazolias等,2024)。本研究证实,BF839联合抗PD-1治疗不仅能增加功能性CD8+T细胞浸润,还可增强抗PD-1疗效。RNA测序分析显示,BF839组中胞质DNA感受(cGAS-STING)通路显著激活。
目前PD-L1表达和肿瘤突变负荷等生物标志物已被证实与ICIs疗效相关。近年来,肠道菌群多样性作为影响ICIs治疗异质性的关键因素受到广泛关注(Zhang等,2021)。研究共识表明,抗生素使用会导致特定菌群缺失及多样性下降(Rashidi等,2021),这种菌群紊乱会显著降低化疗和免疫治疗效果(Erttmann等,2022;He等,2021)。在接受ICIs治疗的肿瘤患者中,抗生素使用与无进展生存期(PFS)和总生存期(OS)呈负相关,证实和谐的肠道菌群生态系统是发挥抗肿瘤效应的必要条件(Derosa等,2018;Cheung等,2021)。通过益生菌调节抗生素相关菌群失调和多样性,成为改善ICIs治疗的潜在策略(Routy等,2018)。本研究发现,非BF839治疗组小鼠的肠道菌群多样性显著低于BF839治疗组。临床数据显示,口服BF839可显著提高晚期实体瘤患者对ICIs的治疗应答,这种效应在长期治疗组尤为明显。我们推测短期BF839治疗可能无法形成有效的益生菌定植,其最佳治疗周期仍有待确定。作为国内临床常用于改善便秘、腹泻等菌群失调症状的益生菌制剂,BF839在免疫治疗过程中具有调节肠道菌群失衡的潜在应用价值。
本研究存在若干局限性。首先,所有受试者均来自单一中心,未来需开展多中心队列研究以进一步验证结果,因为遗传背景、饮食习惯、合并症等因素均会影响肠道菌群多样性(Lozupone等,2012;David等,2014;Wang等,2024)。其次,由于研究属于回顾性设计,我们未能获取患者的粪便样本和肿瘤活检标本,因此无法分析益生菌定植情况和肿瘤微环境特征。最后,在小鼠模型中,虽然证实STING通路参与BF839促进抗肿瘤免疫的过程,但其分子机制仍需深入探究。
综上所述,我们的数据表明益生菌BF839通过cGAS-STING通路调控肿瘤抑制效应。BF839通过改善肠道菌群多样性和促进CD8+T细胞浸润来增强ICIs敏感性。本研究揭示了调节肠道菌群在ICIs治疗肿瘤患者中的治疗潜力,并为提高ICIs疗效提供了新策略。
原文下载:
数据可用性声明
本研究生成的序列数据已上传至百度网盘。可通过链接https://pan.baidu.com/s/1lpMuHppiYPxNE_nO0XXkWw访问,提取码为bf83。若有合理需求,支持本研究结果的数据可从通讯作者处获取。
伦理声明
涉及人类的研究已获得广州医科大学附属第二医院机构伦理审查委员会的批准。研究按照当地法律法规和机构要求进行。参与者均提供了书面知情同意书以参与本研究。动物研究已获得广州医科大学附属第二医院机构动物护理与使用委员会的批准。该研究同样依照当地法律法规和机构要求开展。
作者贡献
KP:数据整理、形式分析、资金获取、调查研究、方法学、验证、初稿撰写;YL:数据整理、形式分析、调查研究、方法学、验证、初稿撰写;QY:调查研究、方法学、文稿修订;PY:调查研究、方法学、文稿修订;TZ:可视化、文稿修订;CL:可视化、文稿修订;YD:概念设计、项目管理、文稿修订;JC:概念设计、项目管理、文稿修订。
资金支持
作者声明,本研究及本文的发表获得了资金支持。这项工作得到了广州市科技基金(2023A04J0591)和广州医科大学科研提升计划(2024)的资助。
致谢
我们感谢中山大学肿瘤防治中心的夏小军博士慷慨提供小鼠黑色素瘤B16和B16-STING-KO细胞 。
利益冲突
作者声明,在开展这项研究过程中不存在任何可被视为潜在利益冲突的商业或财务关系。
生成式人工智能声明
作者声明在撰写本论文过程中未使用生成式人工智能工具。
出版方声明
本文所表达的所有观点仅为作者个人观点,不一定代表其所属机构、出版方、编辑和审稿人的观点。本文中可能涉及评估的任何产品,或其制造商可能提出的任何声明,出版方不提供保证或背书。
补充材料
本文的补充材料可在以下网址在线获取:https://www.frontiersin.org/articles/10.3389/fmicb.2025.1523754/full#supplementary-material
图S1 | 412个差异表达基因的热图。
图S2 | PBS组和BF839组中差异表达基因(Fold Change > 2或Fold Change < 0.5且p值< 0.05)的基因本体(GO)分析 。
参考文献
Brezina, S., Borkovec, M., Baierl, A., Bastian, F., Futschik, A., Gasche, N., et al. (2023). Using fecal immmunochemical cartridges for gut microbiome analysis within a colorectal cancer screening program. Gut Microbes 15:2176119. doi: 10.1080/19490976.2023.2176119
Canale, F. P., Basso, C., Antonini, G., Perotti, M., Li, N., Sokolovska, A., et al. (2021). Metabolic modulation of tumours with engineered bacteria for immunotherapy. Nature 598, 662–666. doi: 10.1038/s41586-021-04003-2
Chan, A. T. C., Lee, V. H. F., Hong, R. L., Ahn, M. J., Chong, W. Q., Kim, S. B., et al. (2023). Pembrolizumab monotherapy versus chemotherapy in platinum-pretreated, recurrent or metastatic nasopharyngeal cancer (KEYNOTE-122): an open-label, randomized, phase III trial. Ann. Oncol. 34, 251–261. doi: 10.1016/j.annonc.2022.12.007
Chang, Y., Yuan, L., Liu, J., Muhammad, I., Cao, C., Shi, C., et al. (2020). Dihydromyricetin attenuates Escherichia coli lipopolysaccharide-induced ileum injury in chickens by inhibiting NLRP3 inflammasome and TLR4/NF-kappaB signalling pathway. Vet. Res. 51:72. doi: 10.1186/s13567-020-00796-8
Cheung, K. S., Lam, L. K., Seto, W. K., and Leung, W. K. (2021). Use of antibiotics during immune checkpoint inhibitor treatment is associated with lower survival in hepatocellular carcinoma. Liver Cancer 10, 606–614. doi: 10.1159/000518090
Cortes, J., Rugo, H. S., Cescon, D. W., Im, S. A., Yusof, M. M., Gallardo, C., et al. (2022). Pembrolizumab plus chemotherapy in advanced triple-negative breast Cancer. N. Engl. J. Med. 387, 217–226. doi: 10.1056/NEJMoa2202809
Davar, D., Dzutsev, A. K., McCulloch, J. A., Rodrigues, R. R., Chauvin, J. M., Morrison, R. M., et al. (2021). Fecal microbiota transplant overcomes resistance to anti-PD-1 therapy in melanoma patients. Science 371, 595–602. doi: 10.1126/science.abf3363
David, L. A., Maurice, C. F., Carmody, R. N., Gootenberg, D. B., Button, J. E., Wolfe, B. E., et al. (2014). Diet rapidly and reproducibly alters the human gut microbiome. Nature 505, 559–563. doi: 10.1038/nature12820
Derosa, L., Hellmann, M. D., Spaziano, M., Halpenny, D., Fidelle, M., Rizvi, H., et al. (2018). Negative association of antibiotics on clinical activity of immune checkpoint inhibitors in patients with advanced renal cell and non-small-cell lung cancer. Ann. Oncol. 29, 1437–1444. doi: 10.1093/annonc/mdy103
Derosa, L., and Zitvogel, L. (2022). A probiotic supplement boosts response to cancer immunotherapy. Nat. Med. 28, 633–634. doi: 10.1038/s41591-022-01723-4
Dizman, N., Meza, L., Bergerot, P., Alcantara, M., Dorff, T., Lyou, Y., et al. (2022). Nivolumab plus ipilimumab with or without live bacterial supplementation in metastatic renal cell carcinoma: a randomized phase 1 trial. Nat. Med. 28, 704–712. doi: 10.1038/s41591-022-01694-6
Erttmann, S. F., Swacha, P., Aung, K. M., Brindefalk, B., Jiang, H., Hartlova, A., et al. (2022). The gut microbiota prime systemic antiviral immunity via the cGAS-STING-IFN-I axis. Immunity 55, 847–861.e10. doi: 10.1016/j.immuni.2022.04.006
Forde, P. M., Spicer, J., Lu, S., Provencio, M., Mitsudomi, T., Awad, M. M., et al. (2022). Neoadjuvant Nivolumab plus chemotherapy in resectable lung Cancer. N. Engl. J. Med. 386, 1973–1985. doi: 10.1056/NEJMoa2202170
Geng, Z., Wang, X., Wu, F., Cao, Z., and Liu, J. (2023). Biointerface mineralization generates ultraresistant gut microbes as oral biotherapeutics. Sci. Adv. 9:eade0997. doi: 10.1126/sciadv.ade0997
Giampazolias, E., Pereira da Costa, M., Lam, K. C., Lim, K. H. J., Cardoso, A., Piot, C., et al. (2024). Vitamin D regulates microbiome-dependent cancer immunity. Science 384, 428–437. doi: 10.1126/science.adh7954
Gopalakrishnan, V., Spencer, C. N., Nezi, L., Reuben, A., Andrews, M. C., Karpinets, T. V., et al. (2018). Gut microbiome modulates response to anti-PD-1 immunotherapy in melanoma patients. Science 359, 97–103. doi: 10.1126/science.aan4236
He, Y., Fu, L., Li, Y., Wang, W., Gong, M., Zhang, J., et al. (2021). Gut microbial metabolites facilitate anticancer therapy efficacy by modulating cytotoxic CD8(+) T cell immunity. Cell Metab. 33, 988–1000.e7. doi: 10.1016/j.cmet.2021.03.002
Hu, M., Lin, X., Sun, T., Shao, X., Huang, X., Du, W., et al. (2024). Gut microbiome for predicting immune checkpoint blockade-associated adverse events. Genome Med. 16:16. doi: 10.1186/s13073-024-01285-9
Kennedy, L. B., and Salama, A. K. S. (2020). A review of cancer immunotherapy toxicity. CA Cancer J. Clin. 70, 86–104. doi: 10.3322/caac.21596
Lee, S. H., Cho, S. Y., Yoon, Y., Park, C., Sohn, J., Jeong, J. J., et al. (2021). Bifidobacterium bifidum strains synergize with immune checkpoint inhibitors to reduce tumour burden in mice. Nat. Microbiol. 6, 277–288. doi: 10.1038/s41564-020-00831-6
Li, Z., Xiong, W., Liang, Z., Wang, J., Zeng, Z., Kolat, D., et al. (2024). Critical role of the gut microbiota in immune responses and cancer immunotherapy. J. Hematol. Oncol. 17:33. doi: 10.1186/s13045-024-01541-w
Li, Z., Zhang, Y., Hong, W., Wang, B., Chen, Y., Yang, P., et al. (2022). Gut microbiota modulate radiotherapy-associated antitumor immune responses against hepatocellular carcinoma via STING signaling. Gut Microbes 14:2119055. doi: 10.1080/19490976.2022.2119055
Liang, K., Liu, Q., Li, P., Luo, H., Wang, H., and Kong, Q. (2019). Genetically engineered Salmonella Typhimurium: recent advances in cancer therapy. Cancer Lett. 448, 168–181. doi: 10.1016/j.canlet.2019.01.037
Liu, C., Du, M. X., Xie, L. S., Wang, W. Z., Chen, B. S., Yun, C. Y., et al. (2024). Gut commensal Christensenella minuta modulates host metabolism via acylated secondary bile acids. Nat. Microbiol. 9, 434–450. doi: 10.1038/s41564-023-01570-0
Liu, W., Pi, Z., and Mao, W. (2024). Beyond probiotics: postbiotics sensitize cancer cells to immune checkpoint inhibitors. Trends Cancer 10, 5–7. doi: 10.1016/j.trecan.2023.12.001
Lozupone, C. A., Stombaugh, J. I., Gordon, J. I., Jansson, J. K., and Knight, R. (2012). Diversity, stability and resilience of the human gut microbiota. Nature 489, 220–230. doi: 10.1038/nature11550
Ludford, K., Ho, W. J., Thomas, J. V., Raghav, K. P. S., Murphy, M. B., Fleming, N. D., et al. (2023). Neoadjuvant Pembrolizumab in localized microsatellite instability high/deficient mismatch repair solid tumors. J. Clin. Oncol. 41, 2181–2190. doi: 10.1200/JCO.22.01351
Ma, X., Liang, X., Li, Y., Feng, Q., Cheng, K., Ma, N., et al. (2023). Modular-designed engineered bacteria for precision tumor immunotherapy via spatiotemporal manipulation by magnetic field. Nat. Commun. 14:1606. doi: 10.1038/s41467-023-37225-1
Mao, Y. Q., Huang, J. T., Zhang, S. L., Kong, C., Li, Z. M., Jing, H., et al. (2023). The antitumour effects of caloric restriction are mediated by the gut microbiome. Nat. Metab. 5, 96–110. doi: 10.1038/s42255-022-00716-4
Mattiola, I., and Diefenbach, A. (2023). Regulation of innate immune system function by the microbiome: consequences for tumor immunity and cancer immunotherapy. Semin. Immunol. 66:101724. doi: 10.1016/j.smim.2023.101724
McQuade, J. L., Daniel, C. R., Helmink, B. A., and Wargo, J. A. (2019). Modulating the microbiome to improve therapeutic response in cancer. Lancet Oncol. 20, e77–e91. doi: 10.1016/S1470-2045(18)30952-5
Mok, T., Nakagawa, K., Park, K., Ohe, Y., Girard, N., Kim, H. R., et al. (2024). Nivolumab plus chemotherapy in epidermal growth factor receptor-mutated metastatic non-small-cell lung Cancer after disease progression on epidermal growth factor receptor tyrosine kinase inhibitors: final results of CheckMate 722. J. Clin. Oncol. 42, 1252–1264. doi: 10.1200/JCO.23.01017
Motzer, R. J., Porta, C., Eto, M., Powles, T., Grunwald, V., Hutson, T. E., et al. (2024). Lenvatinib plus Pembrolizumab versus Sunitinib in first-line treatment of advanced renal cell carcinoma: final Prespecified overall survival analysis of CLEAR, a phase III study. J. Clin. Oncol. 42, 1222–1228. doi: 10.1200/JCO.23.01569
Park, S., Kim, T. M., Han, J. Y., Lee, G. W., Shim, B. Y., Lee, Y. G., et al. (2024). Phase III, randomized study of Atezolizumab plus bevacizumab and chemotherapy in patients with EGFR-or ALK-mutated non-small-cell lung Cancer (ATTLAS, KCSG-LU19-04). J. Clin. Oncol. 42, 1241–1251. doi: 10.1200/JCO.23.01891
Qin, S., Chen, Z., Fang, W., Ren, Z., Xu, R., Ryoo, B. Y., et al. (2023). Pembrolizumab versus placebo as second-line therapy in patients from Asia with advanced hepatocellular carcinoma: a randomized, double-blind, phase III trial. J. Clin. Oncol. 41, 1434–1443. doi: 10.1200/JCO.22.00620
Rashidi, A., Ebadi, M., Rehman, T. U., Elhusseini, H., Nalluri, H., Kaiser, T., et al. (2021). Gut microbiota response to antibiotics is personalized and depends on baseline microbiota. Microbiome 9:211. doi: 10.1186/s40168-021-01170-2
Routy, B., Gopalakrishnan, V., Daillere, R., Zitvogel, L., Wargo, J. A., and Kroemer, G. (2018). The gut microbiota influences anticancer immunosurveillance and general health. Nat. Rev. Clin. Oncol. 15, 382–396. doi: 10.1038/s41571-018-0006-2
Routy, B., Le Chatelier, E., Derosa, L., Duong, C. P. M., Alou, M. T., Daillere, R., et al. (2018). Gut microbiome influences efficacy of PD-1-based immunotherapy against epithelial tumors. Science 359, 91–97. doi: 10.1126/science.aan3706
Roy, R., and Singh, S. K. (2024). The microbiome modulates the immune system to influence cancer therapy. Cancers (Basel) 16:779. doi: 10.3390/cancers16040779
Sehrawat, N., Yadav, M., Singh, M., Kumar, V., Sharma, V. R., and Sharma, A. K. (2021). Probiotics in microbiome ecological balance providing a therapeutic window against cancer. Semin. Cancer Biol. 70, 24–36. doi: 10.1016/j.semcancer.2020.06.009
Simpson, R. C., Shanahan, E. R., Batten, M., Reijers, I. L. M., Read, M., Silva, I. P., et al. (2022). Diet-driven microbial ecology underpins associations between cancer immunotherapy outcomes and the gut microbiome. Nat. Med. 28, 2344–2352. doi: 10.1038/s41591-022-01965-2
Sofi, M. H., Wu, Y., Ticer, T., Schutt, S., Bastian, D., Choi, H. J., et al. (2021). A single strain of Bacteroides fragilis protects gut integrity and reduces GVHD. JCI Insight 6:e136841. doi: 10.1172/jci.insight.136841
Spencer, C. N., McQuade, J. L., Gopalakrishnan, V., McCulloch, J. A., Vetizou, M., Cogdill, A. P., et al. (2021). Dietary fiber and probiotics influence the gut microbiome and melanoma immunotherapy response. Science 374, 1632–1640. doi: 10.1126/science.aaz7015
Szostak, N., Handschuh, L., Samelak-Czajka, A., Tomela, K., Pietrzak, B., Schmidt, M., et al. (2024). Gut Mycobiota Dysbiosis is associated with melanoma and response to anti-PD-1 therapy. Cancer Immunol. Res. 12, 427–439. doi: 10.1158/2326-6066.CIR-23-0592
Taniguchi, S., Shimatani, Y., and Fujimori, M. (2016). Tumor-targeting therapy using gene-engineered anaerobic-nonpathogenic Bifidobacterium longum. Methods Mol. Biol. 1409, 49–60. doi: 10.1007/978-1-4939-3515-4_5
Tomita, Y., Ikeda, T., Sakata, S., Saruwatari, K., Sato, R., Iyama, S., et al. (2020). Association of Probiotic Clostridium butyricum therapy with survival and response to immune checkpoint blockade in patients with lung Cancer. Cancer Immunol. Res. 8, 1236–1242. doi: 10.1158/2326-6066.CIR-20-0051
van Nood, E., Dijkgraaf, M. G., and Keller, J. J. (2013). Duodenal infusion of feces for recurrent Clostridium difficile. N. Engl. J. Med. 368:2145. doi: 10.1056/NEJMc1303919
Vetizou, M., Pitt, J. M., Daillere, R., Lepage, P., Waldschmitt, N., Flament, C., et al. (2015). Anticancer immunotherapy by CTLA-4 blockade relies on the gut microbiota. Science 350, 1079–1084. doi: 10.1126/science.aad1329
Wang, Y., Choo, J. M., Richard, A. C., Papanicolas, L. E., Wesselingh, S. L., Taylor, S. L., et al. (2024). Intestinal persistence of Bifidobacterium infantis is determined by interaction of host genetics and antibiotic exposure. ISME J. 18:wrae107. doi: 10.1093/ismejo/wrae107
Wang, Y., Ma, R., Liu, F., Lee, S. A., and Zhang, L. (2018). Modulation of gut microbiota: a novel paradigm of enhancing the efficacy of programmed Death-1 and programmed death Ligand-1 blockade therapy. Front. Immunol. 9:374. doi: 10.3389/fimmu.2018.00374
Wolter, M., Grant, E. T., Boudaud, M., Steimle, A., Pereira, G. V., Martens, E. C., et al. (2021). Leveraging diet to engineer the gut microbiome. Nat. Rev. Gastroenterol. Hepatol. 18, 885–902. doi: 10.1038/s41575-021-00512-7
Yang, Y. (2015). Cancer immunotherapy: harnessing the immune system to battle cancer. J. Clin. Invest. 125, 3335–3337. doi: 10.1172/JCI83871
Zeng, T., Deng, Y. H., Lin, C. H., Chen, X. X., Jia, H. X., Hu, X. W., et al. (2024). A randomized trial of Bacteroides fragilis 839 on preventing chemotherapy-induced myelosuppression and gastrointestinal adverse effects in breast cancer patients. Asia Pac. J. Clin. Nutr. 33, 23–32. doi: 10.6133/apjcn.202403_33(1).0003
Zhang, F., Ferrero, M., Dong, N., D'Auria, G., Reyes-Prieto, M., Herreros-Pomares, A., et al. (2021). Analysis of the gut microbiota: An emerging source of biomarkers for immune checkpoint blockade therapy in non-small cell lung Cancer. Cancers (Basel) 13:2514. doi: 10.3390/cancers13112514
Zheng, D. W., Li, R. Q., An, J. X., Xie, T. Q., Han, Z. Y., Xu, R., et al. (2020). Prebiotics-encapsulated probiotic spores regulate gut microbiota and suppress Colon Cancer. Adv. Mater. 32:e2004529. doi: 10.1002/adma.202004529
Zhou, S., Gravekamp, C., Bermudes, D., and Liu, K. (2018). Tumour-targeting bacteria engineered to fight cancer. Nat. Rev. Cancer 18, 727–743. doi: 10.1038/s41568-018-0070-z
Zitvogel, L., Derosa, L., and Kroemer, G. (2022). Modulation of cancer immunotherapy by dietary fibers and over-the-counter probiotics. Cell Metab. 34, 350–352. doi: 10.1016/j.cmet.2022.02.004
关键词:脆弱拟杆菌(Bacteroides fragilis),肠道菌群,肿瘤微环境,免疫检查点抑制剂,免疫治疗
引用格式:Peng K, Li Y, Yang Q, Yu P, Zeng T, Lin C, Deng Y and Chen J (2025) The therapeutic promise of probiotic Bacteroides fragilis (BF839) in cancer immunotherapy. Front. Microbiol. 16:1523754. doi: 10.3389/fmicb.2025.1523754
收稿日期:2024年11月6日;接受日期:2025年3月18日;出版日期:2025年3月31日。
特邀编辑:
K. B. Arun,印度基督大学
评审专家:
Yiming Wang,澳大利亚南澳健康与医学研究所
Scott Christley,美国德克萨斯大学西南医学中心
Yu-gang Huang,中国湖北医药学院
版权声明:© 2025彭、李、杨、余、曾、林、邓和陈。这是一篇基于知识共享署名许可协议(CC BY)发布的开放获取文章。根据公认的学术规范,只要注明原始作者和版权所有者,并引用本刊原始发表,允许在任何论坛进行使用、传播或复制。任何不符合这些条款的使用、传播或复制均不被允许。
*通讯作者:邓宇虹,1376708863@qq.com;陈静琦,chenjingqi2002@163.com
†这些作者对研究工作贡献均等


