从“打嗝排气”到正常排气:一例SIBO患者的三阶段饮食+微生态干预复盘
作者:何凯茵
SIBO
SIBO(小肠细菌过度生长),简单说就是本应菌群稀少、内容物快速通过的小肠,因动力变慢、胃酸屏障下降或药物影响,导致细菌“扎堆发酵”。典型表现为餐后腹胀、嗳气,虽有人腹泻,但“没腹泻≠不是SIBO”。治疗需打组合拳:通过低FODMAP或SCD饮食减少发酵底物;用抗生素/抗菌方案降低细菌负荷;配合促动力及屏障修复——这一步常被低估,却直接决定复发与否;最后重建饮食多样性,实现长期稳定。
案例展示
有些腹胀特别 “磨人”:既不便秘也不腹泻,检查报告常常显示 “没大问题”,可只要一吃米饭、面条或甜点,肚子就像被吹起来的气球 —— 胀、顶、嗳气不停,只能靠打嗝才能稍微舒服点。24 岁的尚先生(化名),就被这种 “气” 困扰了很久。
他曾为了减重,尝试过生酮饮食配合司美格鲁肽,加上大量运动,成功减重约70斤。但问题也随之而来:司美格鲁肽本身会抑制胃肠蠕动,停药三个月后,他的腹胀症状明显加重。这是一个关键提示:当胃肠动力被按下“慢速键”,小肠更容易出现细菌过度生长(SIBO),进而导致发酵与气体滞留。
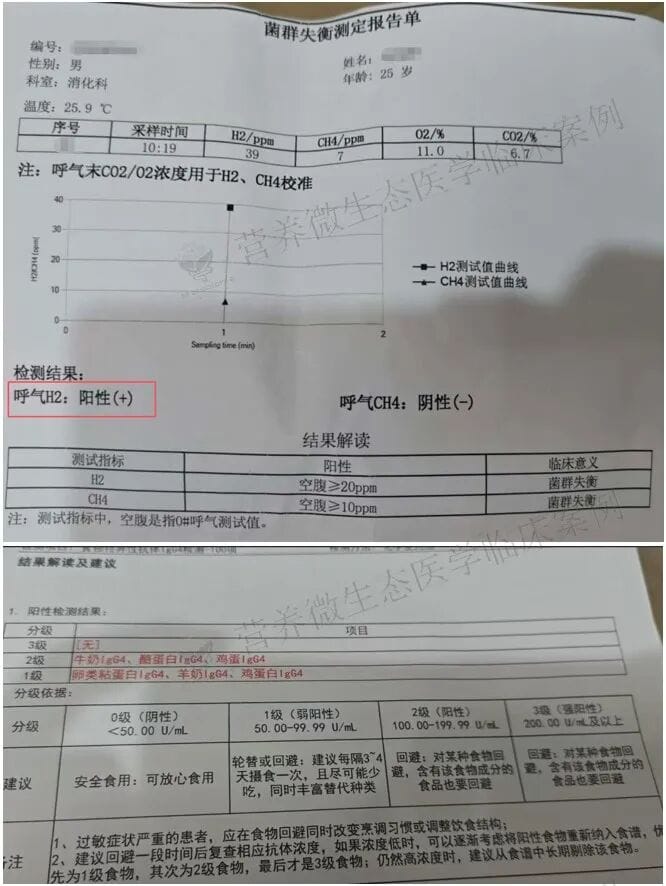
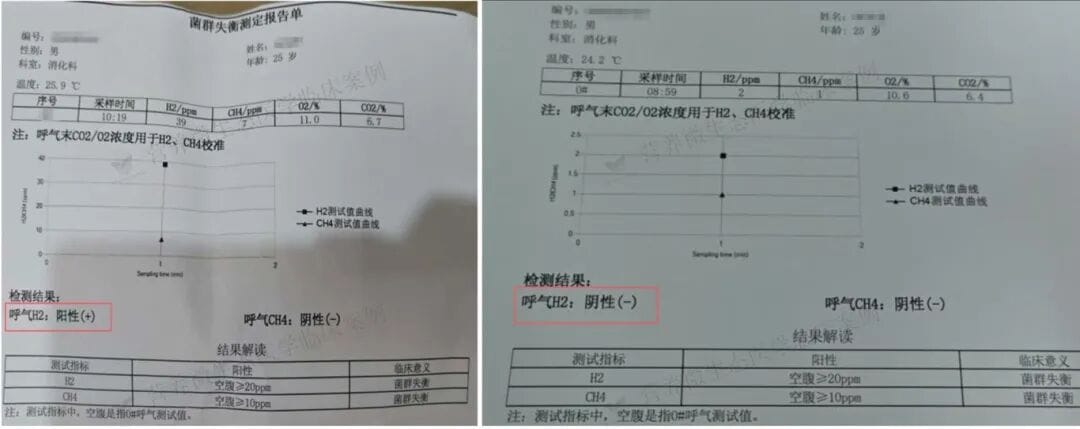
尚先生的症状很典型:餐后胀气(尤其吃碳水时)、嗳气,没有腹泻或便秘,但早期 “气往上顶”,只能靠打嗝排气。检查结果证实了问题 —— 呼气 H2 阳性,提示小肠细菌过度生长(SIBO);食物特异性抗体 IgG4 显示牛奶、酪蛋白、鸡蛋等 2 级过敏;童年还有频繁使用抗生素的历史,肠道菌群 “底子差”。
尚先生他给我最大的印象是“久病成医”——为了解决问题,他做过很多尝试:为了解决愈发严重的腹胀问题,他曾做过两次FMT(粪菌移植),但症状不但没缓解,反而更糟。对于“动力慢+小肠发酵”型人群,盲目移植可能适得其反。此外,他也尝试过低FODMAP饮食、小檗碱搭配牛至油的自然疗法杀菌,效果均不理想。
他多次“努力”带来的反效果,让我这个医生也感触颇深——治疗的突破口,往往不是更狠的忌口,也不是更猛的“杀菌”,而是想尽办法,让体内的气体终于“往下走”,让肠蠕动真正回来。因此,我决定把治疗思路拆解开来,分步走:
第一阶段:先控发酵,再谈修复
饮食上,先尝试低 FODMAP 但效果不佳,转而用更严格的 SCD 饮食(特殊碳水化合物饮食)控制可发酵底物;同时用利福西明 + 黄连素抗菌。配合消化酶、维生素 D、镁、鱼油等补充。杀菌后,胀气明显改善,但仍有残留 —— 说明发酵负荷下降能缓解症状,但仅靠控底物和杀菌还不够。
第二阶段:拉回动力,让气体往下走
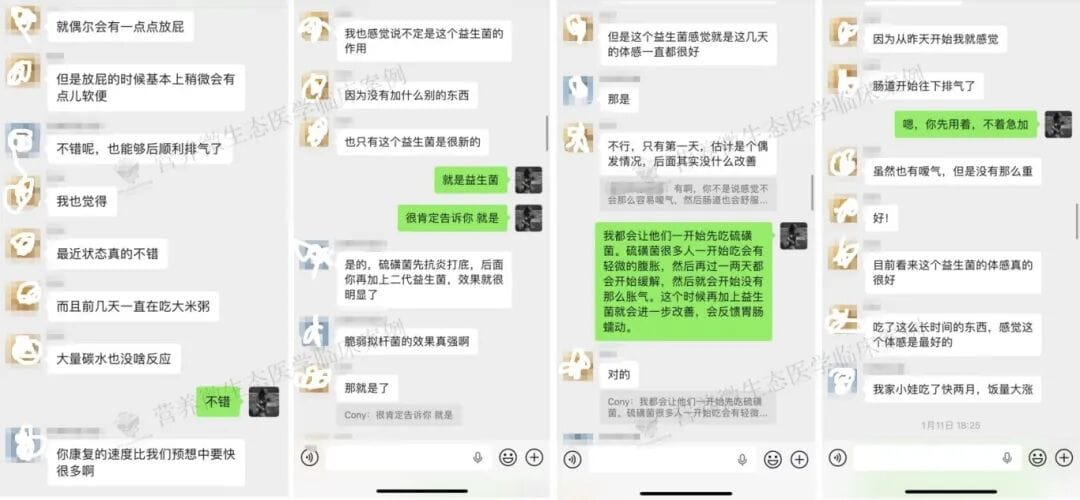
这是真正的转折点:在继续 SCD 饮食的基础上,加入 “硫磺菌”(朱红硫磺菌 ttys-997)。尚先生很快反馈:打嗝明显减少,肚子开始 “动起来”,能正常排气了。后续联用脆弱拟杆菌 BF839(1 包 / 天),胀气进一步减轻,仅在疲劳或压力大时轻微发作,喝姜水就能缓解。
第三阶段:复食重建,不复发才是关键
症状平稳后,真正的考验是如何回归正常生活、如何不复发。我们开始逐步引导他引入更多种类食物,让肠道接触丰富底物,以重建菌群多样性。补充剂方面保留“硫磺菌+脆弱拟杆菌BF839”,并加入三丁酸甘油酯,以修复肠屏障、为菌群提供稳定环境。结果如期:他不仅能吃碳水,连蒜、洋葱这类易产气食物也不再胀气,只要不吃锅包肉这类 “正常人也会胀” 的食物,基本无不适。尚先生的心态也从 “怕吃” 变成 “会吃”,生活质量大幅提升。
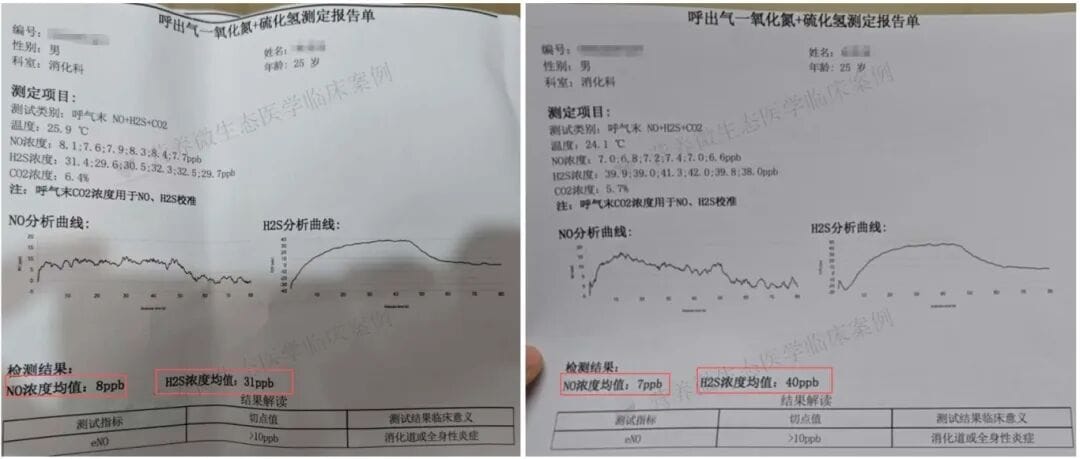
再看复查报告:治疗前他的呼气氢气阳性,治疗后转为阴性。硫化氢浓度从31ppb升至40ppb,一氧化氮从8ppb降至7ppb。这些数字背后,是肠道微生态的真实改变——产气模式变了,气体也能顺畅下行。
2026年1月,尚先生送来一面锦旗:“你相信光吗?不!我相信何医生!”这句俏皮话,其实是患者对我们这种“不唯书、不唯上、只唯实”的个体化治疗思路的最高褒奖。

复盘这个案例,我有几点临床启发:
1) 别只盯“杀菌”,动力是底层变量
当动力慢,细菌和气体就更容易滞留;治疗很容易陷入“杀一波—好几天—又复发”的循环。
这例最漂亮的节点,是气体从上行变下行。
2) 低FODMAP不是万能钥匙,SCD也不是人人适合
饮食是工具,不是信仰。这例里低FODMAP无效,换策略才推进;也提醒我们:症状变化要驱动调整,而不是让患者硬扛。
3) 复食与多样性,才是“长期不复发”的开始
很多患者在“有效饮食”里越吃越少,最后营养、情绪、社交全受损,反而更容易波动。第三阶段的重点,是把患者带回可持续的正常生活。
专业分析
尚先生的干预过程,最值得剖析的一点是:为什么他之前“杀菌”有效但短暂,而这次却能真正稳住?关键在于找准了“动力”这个底层变量。司美格鲁肽的使用是关键诱因之一:作为GLP-1受体激动剂,它通过抑制胃肠蠕动延缓胃排空,当移行性复合运动(MMC)被削弱,小肠的“清扫波”功能即告失效,细菌得以过度增殖并发酵产气,而这些气体本身又会进一步抑制肠蠕动[1]。单纯杀菌之所以效果短暂,是因为只清除了当下的细菌,却未恢复MMC功能。
从“气往上行”到“气往下走”的转变,代表了肠道运动模式的根本逆转。当动力严重障碍时,气体在小肠内积聚、肠腔压力增高,迫使气体向上逆行导致嗳气;当气体能够顺畅下行,意味着小肠内压力梯度恢复正常,节段性蠕动开始协调。
微生态制剂的选择起到关键作用。硫磺菌(朱红硫磺菌ttys-997)通过快速改善消化道炎症、提升有益菌丰度、降低有害菌以修复肠道屏障,促进肠道蠕动恢复[2-3]。联用的脆弱拟杆菌BF839则通过竞争性抑制病原菌定植、分泌丁酸为肠上皮细胞提供能量,同时调节Treg细胞功能,帮助重建免疫耐受[4-8]。两者协同,既解决了“动力慢”的底层问题,又为菌群重建创造了生态位。
饮食调整的边界同样值得关注,其转折点在于第三阶段成功复食。加入三丁酸甘油酯,利用其作为丁酸前体的特性,缓慢释放丁酸以抑制肠道炎症、上调紧密连接蛋白(如ZO-1和Occludin)修复肠屏障,同时增加产短链脂肪酸菌(如双歧杆菌)丰度、抑制条件致病菌,从而为菌群重建创造有利环境[9]。当屏障修复、动力恢复后,再逐步引入多样性底物,从而实现可持续的缓解。
参考文献
[1]Sun Y, Veccia D, Liu B D X, et al. Diagnostic Evaluation of an Increased Risk of Developing Small Intestinal Bacterial Overgrowth Associated with Glucagon-like Peptide-1 (GLP-1) Receptor Agonists and Dual GLP-1/GIP Receptor Agonists: A Global Retrospective Multicenter Cohort Analysis[J]. Diagnostics, 2025, 15(17): 2264.
[2]孙长春.一株朱红硫磺菌及其在治疗消化道溃疡和结肠炎中的应用[P].中国:ZL 202110330475.7,2021,24(03).
[3]Zhao H, Liu L, Liu N, et al. Laetiporus Sulphureus polysaccharides ameliorate chronic alcoholic liver disease by activating p62/Nrf2, AMPK pathways and reshaping gut microbiota[J]. Food Science and Human Wellness, 2024.
[4]Hu J, Chen J, Xu X, Hou Q, Ren J, Yan X. Gut microbiota-derived 3-phenylpropionic acid promotes intestinal epithelial barrier function via AhR signaling. Microbiome. 2023 May 8;11(1):102. doi: 10.1186/s40168-023-01551-9
[5]Geng Z, Wang X, Wu F, Cao Z, Liu J. Biointerface mineralization generates ultraresistant gut microbes as oral biotherapeutics. Sci Adv. 2023 Mar 15;9(11):eade0997.
[6]Mazmanian SK, Liu CH, Tzianabos AO, Kasper DL. An immunomodulatory molecule of symbiotic bacteria directs maturation of the host immune system. Cell. 2005 Jul 15;122(1):107-18.
[7]Tong M, Xu J, Li W, et al. A highly conserved SusCD transporter determines the import and species-specific antagonism of Bacteroides ubiquitin homologues. Nat Commun. 2024;15(1):8794. Published 2024 Oct 10.
[8]Buzun E, Hsu CY, Sejane K, Oles RE, Vasquez Ayala A, Loomis LR, Zhao J, Rossitto LA, McGrosso DM, Gonzalez DJ, Bode L, Chu H. A bacterial sialidase mediates early-life colonization by a pioneering gut commensal. Cell Host Microbe. 2024 Feb 14;32(2):181-190.e9.
[9]Yang N, Lan T, Han Y, et al. Tributyrin alleviates gut microbiota dysbiosis to repair intestinal damage in antibiotic-treated mice[J]. PloS one, 2023, 18(7): e0289364.